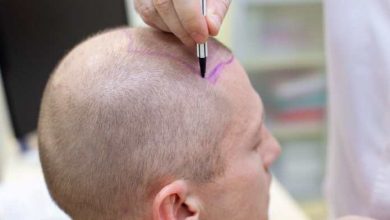
Fiutare il Parkinson a fior di pelle. Ecco il futuro della diagnosi di Parkinson precoce secondo i ricercatori dell’Università di Manchester. Il team di esperti ha sviluppato un «naso elettronico» per scovare i segnali spia della malattia presenti nel sebo della cute. Il progetto, chiamato NoseToDiagnose, è stato ispirato dall’incredibile capacità olfattiva di Joy Milne. L’ex infermiera scozzese per prima ha notato come i malati di Parkinson emanino un particolare odore muschiato. Questo odore aumenta di intensità con l’avanzare della malattia. Grazie al suo fiuto da segugio, i ricercatori britannici hanno identificato le molecole responsabili di questo fenomeno e hanno addestrato il loro dispositivo a riconoscerle. Sapremo qualcosa di più della sua efficacia entro il 2022, quando dovrebbero essere conclusi i test sui pazienti.
In questo articolo
Diagnosi di Parkinson: utile anche la biopsia della pelle
Nel frattempo anche in Italia si è fatta strada l’ipotesi di future diagnosi «a pelle» della malattia neurodegenerativa. Ne parla lo studio pubblicato sulla rivista Brain dall’Università Statale di Milano. I ricercatori hanno collaborato con il Centro Parkinson dell’Ospedale Gaetano Pini-CTO e con la Fondazione Grigioni per il Morbo di Parkinson. Gli scienziati hanno scoperto che le terminazioni nervose nella cute dei pazienti presentano degli aggregati di alfa-sinucleina, la proteina difettosa che solitamente si accumula nel cervello a causa del Parkinson. Questi aggregati potranno essere utili per diagnosticare e monitorare i pazienti nel tempo con una semplice biopsia della pelle, ma non solo. La loro presenza rafforza anche l’ipotesi che il Parkinson insorga alla periferia del sistema nervoso. Solo in un secondo momento si propaga al cervello, scatenando gli effetti che conosciamo.
Parkinson: la situazione in Italia
Quello più evidente è la morte dei neuroni che usano la dopamina per comunicare nelle aree cerebrali deputate al controllo dei movimenti. Massimo Filippi è primario dell’unità di neurologia e del servizio di neurofisiologia dell’IRCCS Ospedale San Raffaele di Milano, nonché professore ordinario di neurologia e direttore della scuola di specializzazione in neurologia presso l’Università Vita-Salute San Raffaele.
«Il Parkinson si manifesta mediamente intorno ai 60 anni di età, soprattutto nel sesso maschile. Solo il 5% dei casi ha esordio giovanile, prima dei 40 anni, e riguarda generalmente forme di origine genetica e familiare. Dopo i 70 anni d’età colpisce l’1-2% della popolazione. In Italia si registrano circa 230.000 pazienti».
Diagnosi di Parkinson: quali sono i sintomi?
Lentezza nei movimenti, rigidità e tremore a riposo sono i classici sintomi che fanno subito scattare l’allarme. I pazienti «iniziano solitamente ad accorgersi della malattia quando il tremore diventa invalidante e le azioni della vita quotidiana come camminare, vestirsi o girarsi nel letto, diventano complesse da svolgere e richiedono tempi aumentati». Quando questo accade, però, significa che la lenta moria dei neuroni del cervello è già cominciata. Per fare una diagnosi più tempestiva, invece, bisognerebbe fare attenzione a segnali molto più sfumati che annunciano la malattia in anticipo.
Diagnosi di Parkinson: disturbi del sonno e dell’olfatto i segni premonitori
«Molti anni prima che si manifestino i deficit motori, infatti, possono comparire sintomi non-motori, come disturbi del sonno, ansia, depressione e disturbi dell’olfatto. L’ideale, per conservare una migliore qualità di vita, sarebbe riuscire a carpire i campanelli d’allarme quando ancora il quadro motorio risulta lievemente alterato, così da anticipare la presa in carico e il trattamento». Alla diagnosi si arriva valutando la presenza di bradicinesia. Si tratta della riduzione della velocità e dell’ampiezza del movimento con la ripetizione del gesto, associata a tremore a riposo o rigidità. È comunque necessario ricorrere anche a esami strumentali e test specifici, per escludere altre patologie neurologiche apparentemente simili ma differenti dal Parkinson, i cosiddetti parkinsonismi (vedi box qui sotto).
Dopo la diagnosi di Parkinson, farmaci efficaci per una quindicina di anni
Una volta accertata la malattia, il trattamento si basa principalmente sull’impiego di farmaci sostitutivi della dopamina che alleviano i sintomi. Purtroppo però non arrestano la progressiva degenerazione del cervello. «Dalla fine degli anni Sessanta, da quando cioè si è scoperto il legame tra Parkinson e il deficit di dopamina, la somministrazione del suo precursore, la levodopa, costituisce il cardine del trattamento. Questa molecola è infatti capace di raggiungere i centri motori cerebrali dove viene convertita nel neurotrasmettitore dopamina, alleviando la sintomatologia».
Non solo levodopa
«Attualmente la levodopa è disponibile in formulazioni che la combinano a particolari principi attivi per rallentarne il metabolismo. Prolungare il tempo di vita del farmaco nell’organismo significa ridurre al minimo la dose necessaria. Con lo stesso scopo, ma tramite meccanismi differenti, vengono usati i farmaci inibitori delle COMT (catecol-O-metiltransferasi). Sono molecole come opicapone, tolcapone e entacapone e hanno come obiettivo quello di prolungare l’efficacia della levodopa e ridurne gli effetti collaterali».
Un’altra classe di farmaci che serve ad aumentare la dopamina nel cervello è quella degli inibitori delle MAO-B (mono ammino ossidasi). Rasagilina e selegilina, secondo alcuni studi, svolgerebbero anche un ruolo neuroprotettivo ritardando la neurodegenerazione. In alternativa o in aggiunta alla levodopa sono disponibili infine farmaci dopaminoagonisti (come ropinirolo, pramipexolo e rotigotina) che attivano direttamente i recettori della dopamina a livello cerebrale e hanno una durata d’azione in media più lunga rispetto alla levodopa, anche se causano spesso effetti collaterali.
Farmaci anti Parkinson ed effetti collaterali
«I farmaci permettono di avere un buon compenso dei deficit motori per una quindicina di anni in media. Poi è inevitabile che la loro efficacia inizi a calare, perché si riduce progressivamente il numero di neuroni in grado di usare la dopamina». Per questo motivo, col passare del tempo, possono manifestarsi effetti collaterali anche molto invalidanti. I principali sono l’insorgenza di movimenti del tutto involontari (discinesie) e il cosiddetto fenomeno on-off. In questo caso il paziente passa rapidamente da una buona motilità a momenti di blocco motorio non appena cala l’effetto della singola somministrazione.
Il futuro è della teleassistenza
«Per migliorare le performance motorie e ritardare la necessità di aumentare il dosaggio dei farmaci la fisioterapia rappresenta uno strumento validissimo». La riabilitazione motoria migliora la destrezza manuale, il cammino e l’equilibrio. in questo modo si riduce il rischio di cadute, inoltre potenzia le capacità cognitive del cervello, aiutandolo a riorganizzare le sue connessioni.
«Recentemente è cresciuto anche l’interesse per attività ludico-sportive come il Tai chi o la danza. Possono infatti stimolare i pazienti a una maggiore partecipazione in contesti sociali che sono spesso evitati». Una grande novità è rappresentata dall’impiego nella riabilitazione delle nuove tecnologie, come robot e realtà virtuale, per rendere gli esercizi fisici e cognitivi più coinvolgenti e stimolanti.
«La tecnologia oggi ci permette anche di supportare il paziente a distanza. Proprio durante l’emergenza coronavirus abbiamo avuto la possibilità di testare l’efficacia della teleassistenza con il servizio ParkinsonCare, ottenendo dati molto promettenti. La teleassistenza sembra funzionare, dando speranza per una rete virtuale di medicina come modello anche per il futuro».
La neurostimolazione
Quando farmaci e riabilitazione non bastano più per avere un buon controllo dei sintomi, allora si può considerare l’opzione della neurostimolazione. La procedura prevede l’impianto di una sorta di pacemaker per il cervello. Inserito sotto cute vicino alla clavicola, va a stimolare i neuroni con deboli impulsi elettrici erogati da elettrodi. I medici li impiantano attraverso un intervento neurochirurgico nel cervello, a livello della regione del nucleo subtalamico o del globo pallido. Per fare questo trattamento «è necessario che la malattia sia in fase avanzata ma non troppo, e che il paziente sia ancora indenne dal punto di vista cognitivo. L’intervento di impianto prevede che sia sveglio e collaborativo in sala operatoria». Questo trattamento hi-tech mira a conquistare anni in più di buona funzionalità motoria. In alcuni casi riesce a garantire risultati migliori della terapia farmacologica, ma neppure questo rappresenta una soluzione definitiva.
L’immunoterapia
La svolta, però, potrebbe essere dietro l’angolo: si chiama immunoterapia. «Questo trattamento, ancora in fase sperimentale, si basa sulla somministrazione endovenosa di anticorpi monoclonali. Riescono ad attivare il sistema immunitario del paziente per indurlo a ripulire il cervello dagli accumuli di alfa-sinucleina. Sono da poco cominciati i primi test sull’uomo, anche in Italia, e ci sono grandi aspettative. Il meccanismo terapeutico è simile a quello già impiegato con successo nella cura di alcuni tipi di tumore. In campo neurologico, è già usato sempre in via sperimentale contro l’Alzheimer».